Synthèse publiée le : 13/05/2019
Synthèse : Perspective d’utilisation des données omiques en évaluation des risques sanitaires :
du concept vers l’opérationnalité
De l’étude de l’expression génique à celle du métabolisme, les disciplines omiques, se sont largement développées ces dernières années et peuvent dorénavant apporter des informations plus exhaustives pour l’évaluation des risques sanitaires, en particulier pour la classification et le regroupement des substances, l’identification des modes d’action, la construction de toxicités relatives, mais aussi pour mieux caractériser l’exposome chimique. Bien qu’il subsiste encore des challenges analytiques et méthodologiques, ces données omiques commencent déjà à être utilisées pour produire des valeurs de référence et pourront être intégrées aux approches réglementaires.
En science de la vie, la racine « ome » se réfère aux approches holistiques[1]. L’idée de base des disciplines omiques consiste à appréhender la complexité du vivant dans son ensemble, au moyen de méthodes les moins restrictives possibles sur le plan descriptif. Elles permettent de caractériser les molécules à différents niveaux d’organisation biologiques traduisant des structures, des fonctions ou des dynamiques fondamentales de l’organisme vivant – transcriptome (expression/régulation génique), protéome (protéines), métabolome (métabolites), lipidome (lipides), microbiome (microbiote) – en vue de comparer des groupes d’individus. Les profils d’expression génique, de protéines, de métabolites ou de lipides ainsi identifiés dans des échantillons seront, dans la suite de cette synthèse, appelés « signatures omiques ». Les disciplines omiques mettent en œuvre des technologies analytiques haut débit et des méthodes statistiques complexes pour analyser un grand nombre de variables simultanément. Leurs applications sont nombreuses : recherche clinique, pharmacologie et toxicologie, biologie végétale et agronomie, nutrition et sécurité alimentaire, épidémiologie environnementale. Les omiques sont particulièrement prometteuses en évaluation des risques, d’une part car la notion de haut débit permet de générer des données quantitatives massives et pour certaines technologies, à faible coût, et d’autre part car ce sont des approches intégratives qui améliorent rapidement les connaissances mécanistiques des substances chimiques. L’objectif de cette synthèse est de présenter l’intérêt qu’apportent les approches omiques pour l’évaluation des risques liés aux substances chimiques (figure).
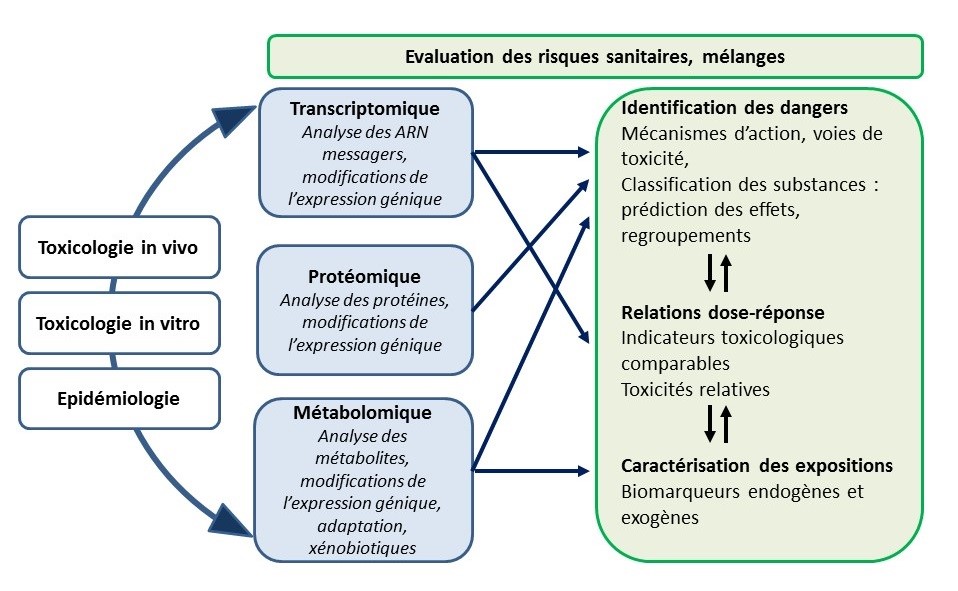
Figure 1. Utilisation des omiques en évaluation des risques
Identification des dangers, l’apport des signatures omiques
Jusqu’à maintenant, les données générées par les omiques ont été très utiles pour améliorer les connaissances sur les voies de toxicité altérées par des substances chimiques pouvant entraîner la survenue d’événements de santé délétères (notion d’adverse outcome pathway) car elles permettent de fournir des données sur les événements moléculaires précurseurs ou intermédiaires à différentes échelles biologiques [1]. Ces données sont particulièrement utiles pour l’évaluation des risques sanitaires liés aux mélanges, notamment pour regrouper des substances en fonction de leurs effets. Cette étape est à ce jour très chronophage et souvent limitée à un nombre de substances restreint, peu représentatif des expositions réelles. L’hypothèse de Steiner selon laquelle des substances ayant des signatures transcriptomiques proches auront une toxicité proche [2] a été testée pour différents groupes de substances : des hépatotoxiques (fongicides triazolés, anti-convulsivants, corticostéroïdes ; perfluorés, fibrates) et des perturbateurs endocriniens reprotoxiques (médicaments, fibrates, fongicides entre autres) qui ont ainsi été regroupés grâce à leurs profils d’expression génique [3, 4]. D’une autre manière, la protéomique a montré des voies d’activation communes chez l’homme pour des pesticides de familles chimiques différentes (triazolés, dicarboxmidies et imidazolés) [5]. Ces éléments sont en faveur d’une meilleure intégration des signatures omiques pour décloisonner les groupes de substances pris en compte dans l’évaluation des risques des mélanges. Aujourd’hui c’est chose faite avec TOXsIgN, qui permet le dépôt en ligne et le stockage des signatures omiques générées par la communauté scientifique. À ce jour, plus de 700 projets correspondant à plus de 400 composés et 8 000 signatures sont disponibles pour faciliter leur exploitation. Cette base a vocation à être élargie à l’ensemble des signatures omiques [6].
Évaluation des relations dose-réponse, des « benchmark doses » aux facteurs de toxicité relative
Les travaux ont jusqu’à maintenant permis de montrer l’apport de la transcriptomique pour la construction de « benchmark dose » [7, 8], indicateur toxicologique servant de point de départ à la construction de valeurs toxicologiques de référence. La benchmark dose est la dose correspondant à un niveau de réponse fixé a priori, estimée à partir de la modélisation de la relation dose-réponse. De plus, le fait de pouvoir générer des données reproductibles à moindre coût permet aux omiques de favoriser les approches comparatives de toxicité, utile pour étudier les mélanges.
Par exemple, les modèles d’additivité pourraient correctement prédire le potentiel de toxicité relatif des phtalates les uns par rapport aux autres à partir de données d’expression génique [9]. De plus, les profils transcriptomiques pulmonaires de souris exposées à des hydrocarbures aromatiques polycycliques pris individuellement pourraient également prédire la toxicité de mélanges plus complexes [10]. La nouveauté en 2018 concerne un outil open source prometteur, DRomics (package R), qui permet, à partir de données omiques multiples, d’identifier le meilleur modèle de courbe dose-réponse pour générer des benchmark doses pour l’évaluation des risques environnementaux [11].
Caractérisation des expositions, biomarqueurs, métabolomique et exposome
En 2017, les académies de sciences, ingénierie, et médecine américaines pointaient le développement, entre autres, des analyses non ciblées de type métabolomique en expologie et en épidémiologie et recommandaient de participer à l’effort d’intégration de ces différentes données [12]. En effet, la métabolomique peut être considérée comme très prometteuse pour la caractérisation à la fois de biomarqueurs d’effet et d’exposition des populations humaines. Une revue de littérature récente sur des populations exposées à des composés chimiques dans différents contextes (sites pollués, alimentation, travail) a montré que l’exposition chimique était associée à la modification de nombreuses voies métaboliques, et que les signatures métaboliques endogènes présentaient des profils proches pour certains groupes : métaux lourds et HAP, composés chlorés persistants ou non, phtalates par exemple [13]. Toutefois, des limites importantes associées notamment à l’identification des métabolites, qu’ils soient endogènes ou qu’ils proviennent des contaminants de l’environnement, ainsi qu’à la sensibilité analytique pour détecter des métabolites présents à l’état de trace dans les matrices biologiques complexes restent encore à surmonter afin de pourvoir bénéficier pleinement des avantages de cette approche [14]. Enfin, cette année, une application du concept d’exposome a été testée expérimentalement pour améliorer l’évaluation des risques et des impacts associés aux expositions industrielles : en plus de la contamination de l'environnement et de la proximité aux sites industriels, les habitudes alimentaires, le statut socio-économique et la variabilité du métabolisme ont été identifiés comme des déterminants importants du neurodéveloppement des enfants dans ces contextes [15]. Une application de la métabolomique a été réalisée dans le cadre du projet européen EXPOsOMICS pour estimer les effets de la pollution de l’air générée par le trafic automobile dans les villes de Londres et Barcelone sur la composition du métabolome sanguin. Cette étude a permis de mettre en avant, entre autres, une association entre les concentrations en NO2 et une perturbation de la voie de l’acyl-carnitine qui est associée aux maladies cardio-vasculaires [16].
Du côté des institutions et de la régulation
Le centre européen pour l’écotoxicologie et la toxicologie des produits chimiques (ECETOC) est déjà actif sur cette question depuis une décennie (organisation de workshops en 2010, 2013). Fin 2017, il recommandait de développer les bonnes pratiques de laboratoire en vue de mieux standardiser la collecte, le stockage et la conservation des données, et considérait qu’il n’était pas encore possible d’utiliser les omiques en routine dans la réglementation, et que la construction de valeurs sanitaires nécessitait encore beaucoup d’efforts de recherche [17]. Les recommandations émises par l’EFSA fin 2018 considèrent également la standardisation des données comme nécessaire pour utiliser les omiques en routine dans les procédures réglementaires d’évaluation des risques, néanmoins elles vont plus loin et donnent des perspectives concrètes à court et moyen terme grâce aux initiatives internationales maintenant nombreuses [18] :
- Pour les valeurs de référence : dans la proposition de doses critiques, en prenant soin de poursuivre les recherches sur la sensibilité des approches omiques par rapport aux approches classiques et les phénomènes d’adaptation versus toxiques ; et pour l’amélioration des facteurs d’incertitude interespèces (meilleure connaissance de la variabilité interespèces et de pertinence des transpositions animal - homme) ;
- Pour les signatures omiques à utiliser en évaluation des risques : l’association de la transcriptomique à la métabolomique permet à la fois une couverture élevée du génotype et du phénotype et ainsi une bonne pertinence biologique ; la métabolomique permet de plus de mesurer à la fois les métabolites endogènes ou provenant des contaminants de notre environnement.
Ainsi, bien qu’il subsiste encore des challenges analytiques et méthodologiques, les données omiques commencent à être utilisées pour produire des valeurs de référence et pourront dans le futur être intégrées aux approches réglementaires.
Bibliographie
[1] Brockmeier EK, Hodges G, Hutchinson TH. The role of omics in the application of adverse outcome pathways for chemical risk assessment. Toxicol Sci. 2017;158:252-262.
[2] Steiner G, Suter L, Boess F et al. Discriminating different classes of toxicants by transcript profiling. Enivron Health Persp. 2004;112:1236-1248.
[3] Martin MT, Brennan RJ, Hu W et al. Toxicogenomic study of triazole fungicides and perfluoroalkyl acids in rat livers predicts toxicity and categorizes chemicals based on mechanisms of toxicity. Toxicol Sci. 2007;97:595-613.
[4] Darde T, Lecluze E, Becker E et al. ChemPSy: identification, classification and prioritization of novel endocrine disruptors by integrating massive toxicogenomics datasets. Rencontres scientifiques de l'Anses. 14/11/2016.
[5] Kongsbak K, Vinggaard AM, Hadrup N, Audouze K. A computational approach to mechanistic and predictive toxicology of pesticides. ALTEX. 2014;31:11-22.
[6] Darde TA, Gaudriault P, Beranger R, et al. TOXsIgN: a cross-species repository for toxicogenomic signatures. Bioinformatics. 2018:1-7.
[7] Thomas RS, Wesselkamper SC, Wang NCY et al. Temporal concordance between apical and transcriptional points of departure for chemical risk assessment. Toxicol Sci. 2013; 134:180-194.
[8] Farmahin R, Williams A, Kuo B et al. Recommended approaches in the application of toxicogenomics to derive points of departure for chemical risk assessment. Arch Toxicol. 2017;91:2045-2065.
[9] Hannas BR, Lambright CS, Furr J et al. Genomic biomarkers of phthalate-induced male reproductive developmental toxicity: a targeted RT-PCR array approach for defining relative potency. Toxicol Sci. 2012;125:544-557.
[10] Labib S, Williams A, Kuo B, Yauk CL, White PA, Halappanavar S. A framework for the use of single-chemical transcriptomics data in predicting the hazards associated with complex mixtures of polycyclic aromatic hydrocarbons. Arch Toxicol. 2017;91:2599-2616.
[11] Larras F, Billoir E, baillard V et al. DRomics: a turnkey tool to support the use of the dose-response framework for omics data in ecological risk assessment. Environmental Science and Technology. 2018. doi: 10.1021/asc.est.8b04752.
[12] Using 21st Century Science to Improve Risk-Related Evaluations. The National Academies Press, 2017. doi: 10.17226/24635.
[13] Bonvallot N, David A, Chalmel F et al. Metabolomics as a powerful tool to decipher the biological effects of environmental contaminants in humans. Curr Op Toxicol. 2018;8:48-56.
[14] Chetwynd AJ, David A. A review of nanoscale LC-ESI for metabolomics and its potential to improve the metabolome coverage. Talanta, 2018, 182 :380-390
[15] Sarigiannis DA, Karakitsios SP. Addressing complexity of health impact assessment in industrially contaminates sites via the exposome paradigm. Epidemiol Prev. 2018;42(5-6)S1:37-48.
[16] Van veldhoven K, Kiss A, Keski-Rahkonen P et al. Impact of short-term traffic-related air pollution on the metabolome – Results from two metabolome-wide experimental studies. Envi Int. 2019; 123:124-131.
[17] Buesen R, Chorley BN, da Silva Lima B et al. Applying omics technologies in chemicals risk assessment: report of an ECETOC workshop. Regul Toxicol Pharmacol. 2017;91:S3-S13.
[18] Aguilera J, Aguilera-Gomez M, Barrucci F et al. EFSA scientific colloquium 24 – omics in risk assessment: state of the art and next step. 2018. EFSA Event Report. doi: 10.2903/sp.efsa.2018.EN-1512.
Note
[1] Initialement, le terme génomique pour « science qui étudie le génome », a été introduit dans le vocabulaire scientifique à partir du moment où l’on a su séquencer le génome (1995 pour un génome bactérien). L’étymologie provient des termes « génome » et « génétique », génome étant lui-même une association des termes « gène » et « chromosome », proposé dès 1920 en Allemagne. À la fin du xxe siècle, la génomique est rapidement devenue une discipline à part entière dont l’objectif était d’exploiter l’ensemble des données issues du séquençage du génome et de ses profils d’expression (génomique fonctionnelle) (Barouki). Aujourd’hui, on entend par « omiques », l’ensemble de ces disciplines qui permettent d’appréhender la complexité du vivant de manière holistique. Le suffixe « ome » s’adapte parfaitement à ces nouvelles disciplines puisqu’il s’agit dans l’hindouisme ancien de la complétude ou plénitude, son originel à partir duquel l’univers cosmique s’est matérialisé.



