Contaminants
Perturbateurs endocriniens

Julien Caudeville, Pauline Morel, Jérôme Naud, Céline Ménard, Sébastien Denys, Mélina Le Barbier
Santé publique France, Saint-Maurice
Télécharger le PDF de la synthèse
Les analyses d'articles sur le même sujet :
- Absence d’association entre les perturbateurs endocriniens et la fertilité masculine : revue systématique et méta-analyse
- Perturbateurs endocriniens dans les poussières intérieures : évolutions spatio-temporelles des concentrations et exposition humaine associée
- Perturbateurs endocriniens dans l’environnement. Étude de leurs effets sur la santé reproductive des femmes et l’endométriose
Synthèse publiée le : 01/11/2024
SYNTHÈSE :
Priorisation des effets sanitaires dans le cadre du programme de surveillance en lien avec les perturbateurs endocriniens
Santé publique France a engagé un travail de priorisation des effets sanitaires liés aux perturbateurs endocriniens, dans le but de cadrer son programme de surveillance au-delà de la sphère reproductive. La méthode de classement des effets à surveiller prioritairement a combiné à la fois les données de la littérature disponibles ainsi que l'avis d'experts et de parties prenantes du champ via la méthode de consultation Delphi.
Contexte
De nombreuses études ont décrit un lien probable entre l’exposition à certains perturbateurs endocriniens (PE) et diverses pathologies, notamment les troubles de la fertilité et de la reproduction (baisse de la qualité du sperme, augmentation de la fréquence d’anomalies du développement des organes ou de la fonction de reproduction, abaissement de l’âge de la puberté, cancers des testicules) [1].
Santé publique France a mis en place une surveillance épidémiologique nationale pour produire des connaissances scientifiques robustes en appui aux politiques publiques et contribuer à caractériser l’impact sanitaire de l’exposition aux PE, en particulier pour orienter les actions et les mesures de prévention. Une première priorisation des effets possibles en lien avec les PE avait été menée en 2013 sur la base du poids des preuves par Santé publique France, à l’aide d’un réseau constitué de scientifiques internationaux (HUman Reproductive health and Global ENvironment Network : HURGENT) [2]. De premiers indicateurs sur la santé reproductive avaient ainsi été sélectionnés pour renseigner, directement ou indirectement, des tendances et/ou des phénomènes temporels et/ou spatiaux relatifs à un événement de santé reproductive à surveiller pour leur lien avec une exposition aux PE. L’évaluation du poids des preuves avait abouti à « la synthèse formalisée de lignes de preuves, éventuellement de qualités hétérogènes, dans le but de déterminer le niveau de plausibilité d’hypothèses », l’hypothèse ici était l’existence d’un lien entre une exposition aux PE et la survenue d’un effet altérant la santé [1].
Le récent bilan de ce programme montre une altération progressive de la santé reproductive en France et semble globalement en adéquation avec celle constatée au niveau international. Elle peut être soit le témoin d’une augmentation réelle de l’incidence des pathologies, soit le reflet d’un biais lié à une sensibilisation des populations voire des médecins à certaines maladies (meilleures connaissances, détections et prises en charge des pathologies) entraînant un dépistage accru ou une combinaison de ces hypothèses [3].
Les connaissances sur les relations entre PE et altération de la santé évoluent régulièrement, et les associations entre expositions aux PE et effets sur la santé sont toujours discutées avec des niveaux de preuves qui évoluent rapidement. Les PE sont suspectés d’être en lien avec de nombreux autres effets sur la santé que la santé reproductive (altération du système immunitaire, troubles de la thyroïde, cancers hormonaux-dépendants, etc.). Des troubles neurologiques comme l’autisme, la baisse de quotient intellectuel ou des troubles métaboliques, comme le diabète ou l’obésité, sont également suspectés d’être associés à une exposition aux PE [1]. D’un point de vue sociétal, l'impact des substances chimiques, et des PE en particulier, sur l'environnement et la santé constitue une source de préoccupation de plus en plus importante. Pour améliorer les connaissances sur les PE en vue de mieux protéger les citoyens et l'environnement contre leurs effets néfastes, soit par le renforcement de la réglementation, soit par l’amélioration de la prévention, la France a ainsi lancé en 2014 une première Stratégie nationale sur les perturbateurs endocriniens (SNPE). La deuxième stratégie, élaborée en associant l’ensemble des parties prenantes, a été lancée en 2019 [4].
Dans ce contexte, Santé publique France a lancé des travaux de priorisation des effets sur la santé des PE (projet PEPS’PE) inscrit dans le cadre de l’action 46 de la SNPE2, dans le but de définir une nouvelle stratégie de surveillance des effets sanitaires en lien avec les PE au-delà de la santé reproductive. Ces travaux viennent compléter par ailleurs les travaux sur la caractérisation de l’exposition de la population aux PE menés dans le cadre du programme national de biosurveillance pour améliorer la compréhension des déterminants de l’exposition.
Projet PEPS’PE : priorisation des effets sanitaires à surveiller dans le cadre du programme de surveillance des pathologies en lien avec les PE
En l’absence de méthode communément admise pour évaluer le poids des preuves concernant l’association entre l’exposition aux PE et la survenue d’un effet sanitaire, une méthode de priorisation a été mise au point, combinant les données de la littérature disponibles et les résultats d’une consultation élargie à diverses parties prenantes [5].
Lors de cette consultation, le consensus a été recherché selon la méthode Delphi qui offre une méthode systématique de collecte et d'agrégation des jugements d'un groupe de participants pour synthétiser l’information et confronter les avis contradictoires.
La démarche proposée s’appuie sur une classification des effets sanitaires par le panel selon deux critères de priorisation tenant compte de l’aspect scientifique et des préoccupations sociétales : le poids des preuves et l’intérêt épidémiologique et sociétal de mise en place d’une surveillance de l’effet sanitaire. Ce critère est composite et tient compte de trois sous-critères :
- la gravité de l’effet sanitaire ;
- l’évolution de l’incidence de l’effet sanitaire ;
- la préoccupation sociétale à propos de l’effet sanitaire en partie traduite par la consultation des parties prenantes des plans nationaux associés à la thématique (PNSE et SNPE).
Quatre catégories de consensus ont été définies basées sur des pourcentages de réponses :
- consensus fort : ≥ 80 % de réponses identiques ;
- consensus modéré : entre 71 et 79 % de réponses identiques ;
- consensus faible : entre 50 et 70 % de réponses identiques ;
- pas de consensus : < 50 % de réponses identiques.
Pour les questions ayant obtenu moins de 50 % de réponses identiques, il a été considéré qu’aucun consensus n’avait été atteint et l’effet sanitaire concerné n’a pas pu être priorisé.
Plus de 500 personnes ont été identifiées en vue de participer à ce travail de priorisation. Un premier groupe a été formé avec des experts du domaine scientifique français et internationaux (épidémiologistes, toxicologues, cliniciens, etc.) dans le but de répondre aux questions scientifiques. Un deuxième groupe a été formé avec des parties prenantes du champ en vue de répondre sur la préoccupation sociétale (membres du conseil d’administration de Sante publique France, membres de la SNPE1 et SNPE2, associations, etc.).
Parmi les 59 effets sanitaires inclus dans la priorisation, identifiés par une revue de la littérature selon le poids des preuves, 43 effets sanitaires ont pu être évalués lors de la consultation, 16 effets n’ont pas pu être priorisés à l’issue de la consultation, soit par manque de participants (troubles cutanés et oculaires, les troubles surrénaliens, les troubles osseux), soit par absence de consensus (dysfonction érectile, hyperplasie prostatique bénigne, allergies) (tableau 1).
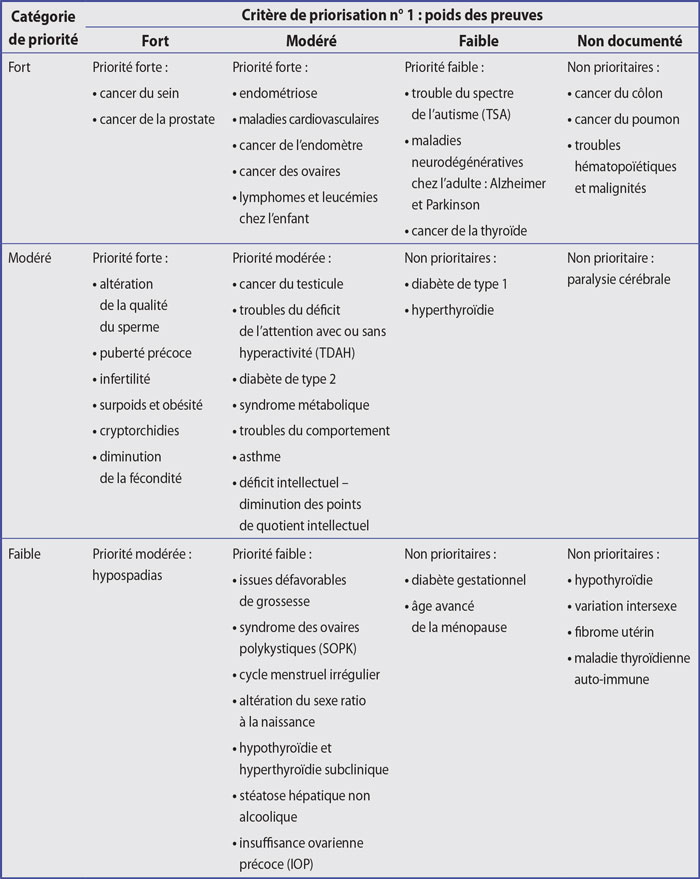
Treize effets sanitaires ont été classés en priorité forte pour la surveillance en lien avec les PE : cancer du sein, cancer de la prostate, endométriose, cryptorchidies, puberté précoce, altération de la qualité du sperme, cancers des ovaires, cancer de l’endomètre, diminution de la fécondité, infertilité, surpoids et obésité, maladies cardiovasculaires, et lymphome et leucémie chez l’enfant. Huit effets sanitaires ont été classés en priorité modérée : cancer du testicule, hypospadias, troubles du neurodéveloppement chez l’enfant (troubles du comportement, déficit intellectuel, trouble déficit de l'attention avec ou sans hyperactivité), troubles métaboliques (diabète de type 2 et syndrome métabolique) et asthme.
Parmi les effets priorisés, plusieurs effets de santé reproductive avaient déjà été priorisés par HURGENT [2], dont certains sont déjà surveillés aujourd’hui par Santé publique France pour leur lien avec les PE (endométriose, cryptorchidies, puberté précoce, altération de la qualité du sperme, cancer du testicule, hypospadias). D’autres effets sanitaires évalués avec une priorité identifiée comme forte ou modérée font déjà l’objet d’une surveillance au sein de l’agence mais pas dans le cadre de la surveillance en lien avec les PE : cancers (cancer des ovaires et de l’endomètre), troubles métaboliques (surpoids et obésité, DT2), maladies cardiovasculaires, asthme et troubles du neurodéveloppement et du neurocomportement chez l’enfant (troubles du comportement, TDAH). Vingt-deux effets sanitaires ont été classés en priorité faible ou non prioritaires.
Intégration des effets sanitaires priorisés dans la surveillance intégrée
Malgré ses limites [5], la méthode Delphi a permis de structurer l’information disponible en tenant compte des connaissances des experts de la thématique et de la préoccupation sociétale afin d'identifier les effets sur la santé devant faire prioritairement l’objet d’une surveillance, à un moment donné, dans un contexte d’incertitudes et de connaissances scientifiques lacunaires. Les résultats de cette consultation permettent ainsi d’apporter des premiers éléments de décision afin d’identifier les effets sanitaires à surveiller en priorité pour leur lien avec les PE. Cette démarche de priorisation est reproductible et permettra d’ajuster dans le temps la sélection d’indicateurs sanitaires étudiés à l’évolution des connaissances et aux données disponibles ainsi qu’aux évolutions des préoccupations sociétales.
Au-delà des effets à considérer, la structuration d’une surveillance dite « intégrée » impliquera de combiner l’ensemble des données disponibles (intégration de données issues d’enquêtes, de cohortes, de registres, de données locales de terrain) afin de produire des indicateurs de surveillance robustes et pour caractériser le lien avec l’exposition. Différentes approches méthodologiques (analyses spatiotemporelles, études écologiques et fardeau environnemental à travers la quantification des impacts sanitaires et l’estimation des couts des maladies notamment) seront développées pour mesurer, analyser et interpréter l’impact des changements environnementaux sur la santé humaine. Cette démarche globale de surveillance intégrée offrira des perspectives intéressantes pour identifier in fine des stratégies et des actions de gestion et prévention efficaces dans un contexte d'incertitude et de connaissances lacunaires. La prochaine étape sera d’évaluer l’efficience de la surveillance de ces effets sanitaires priorisés pour ensuite cadrer le programme de l’agence sur la thématique des PE. Cette analyse consistera à déterminer si des indicateurs fiables et adaptés à la thématique des PE existent déjà ou peuvent être suivis dans le temps et dans l’espace selon une logique de surveillance intégrée.
Références
[1] Gross M, Green RM, Weltje L, Wheeler JR. Weight of evidence approaches for the identification of endocrine disrupting properties of chemicals: Review and recommendations for EU regulatory application. Regul Toxicol Pharmacol 2017; 91 : 20-8.
[2] Le Moal J, Sharpe RM, Jorgensen N, et al. Toward a multicountry monitoring system of reproductive health in the context of endocrine disrupting chemical exposure. Eur J Public Health 2016 ; 26 : 76-83.
[3] Caudeville J, Peyronnet A, Goria S, et al. Bilan et perspectives du programme de surveillance des pathologies en lien avec les perturbateurs endocriniens. Yearbook Environnement, Risque et Santé, 2022 : https://www.jle.com/fr/e-docs/synthese_bilan_et_perspectives_du_programme_de_surveillance_des_pathologies_en_lien_avec_les_perturbateurs_endocriniens_322307/yb_synthese.phtml
[4] Deuxième stratégie nationale sur les perturbateurs endocriniens 2019-2022 : https://sante.gouv.fr/IMG/pdf/snpe_2__2019_2022.pdf
[5] Peyronnet A, Naud J, Caudeville J. Étude PEPS'PE : priorisation des effets sanitaires à surveiller dans le cadre du programme de surveillance en lien avec les perturbateurs endocriniens. Résultats. Santé publique France, 2023, 74 p : https://www.santepubliquefrance.fr/content/download/573041/4065738?version=1
Synthèse publiée le : 17/05/2022
SYNTHESE :
Bilan et perspectives du programme
de surveillance des pathologies en lien avec les perturbateurs endocriniens
Julien Caudeville
Alexia Peyronnet
Sarah Goria
Julie Chesneau
Perrine de Crouy-Chanel
Morgane Stempfelet
Mélina Le Barbier
Céline Ménard
Joëlle Le Moal
Sébastien Denys
Agence Santé publique France, Saint-Maurice
Synthèse publiée le : 12/06/2021
SYNTHÈSE :
L’étude d’imprégnation de la population française
aux perturbateurs endocriniens
(exemples des phtalates et des parabènes)
Clémence Fillol
Santé publique France
Direction Santé Environnement Travail
Saint-Maurice
Synthèse publiée le : 28/05/2018
SYNTHESE : Perturbateurs endocriniens : enjeux et défis autour de leur réglementation en europe
Véronique Ezratty
Aleksandra Piotrowski
Service des Études médicales, EDF, Paris, France
Synthèse publiée le : 01/04/2016
Les perturbateurs endocriniens : 25 ans déjà
Robert Barouki
Inserm UMR-S 1124
Centre universitaire des Saints-Pères
Université Paris Descartes
12, rue de l’École de médecine
75006 Paris
France
Service de biochimie métabolomique et protéomique
Hôpital Necker Enfants malades
149, rue de Sèvres
75015 Paris
France
robert.barouki@parisdescartes.fr






